Glukose-Monitoring: Wohin mit dem Sensor?
 Was bei CGM bedenkenlos klappt, wirkt sich bei FGM auf die Messgenauigkeit aus.
© b4producer – stock.adobe.com
Was bei CGM bedenkenlos klappt, wirkt sich bei FGM auf die Messgenauigkeit aus.
© b4producer – stock.adobe.com
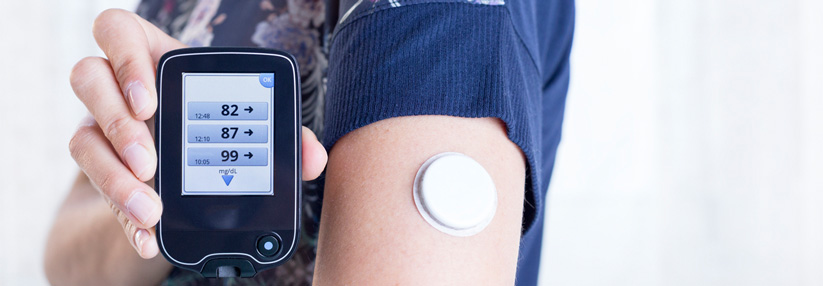
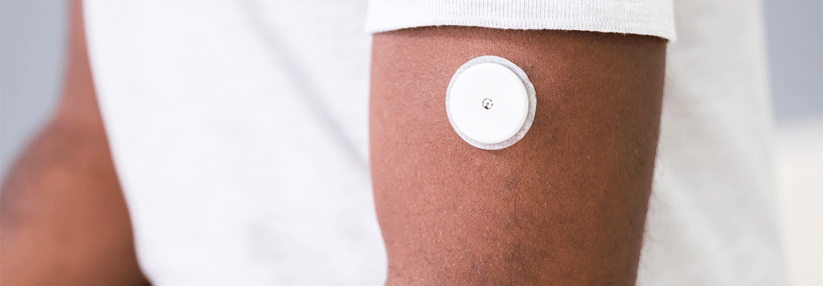
Die Sensoren für das Flash-Glukose-Monitoring (FGM) sollen laut Angaben der Hersteller ausschließlich am Oberarm platziert werden. Patienten interessiert jedoch, ob nicht auch andere Körperstellen möglich sind. Hierzu gibt es auch einen regen Austausch im Internet, berichtete Professor Dr. Manfred Dreyer, niedergelassener Facharzt für Innere Medizin und Diabetologie, Hamburg. Dem wurde nun in einer Studie nachgegangen:¹ 23 Patienten mit Diabetes Typ 1 trugen über einen Zeitraum von 14 Tagen jeweils drei Sensoren gleichzeitig – und zwar am Oberarm, am Oberschenkel und am Bauch. Anschließend wurde bestimmt, wie stark die Sensorenwerte von den verschiedenen Körperstellen von kapillären Glukosemessungen abwichen.
FGM-Messungen am Bauch nicht ausreichend genau
Diese Vergleichswerte wurden anhand von 7-Punkte-Profilen bestimmt. Die mittlere Abweichung am Oberarm betrug 11,8 ± 12,0 % und 12,3 ± 13,8 % am Oberschenkel, die Messungen an den Extremitäten ergaben somit ähnliche Ergebnisse. Am Bauch waren die Werte jedoch deutlich schlechter, so Prof. Dreyer: Hier lag die Abweichung von den Blutglukosewerten bei 18,5 ± 18,4 %.
Zudem lieferten die Messungen am Bauch lediglich in 69,41 % der Fälle ausreichend genaue Werte, an Armen und Beinen waren 85 % der Gewebewerte ausreichend genau. Bisherige FGM-Systeme können daher nicht am Bauch getragen werden, so der Experte. Eine Platzierung am Oberschenkel wäre möglich – allerdings gingen die Sensoren dort in der Studie häufiger verloren.
Viel Fett, wenig Glukose
Quelle:
³ Enderle B et al. J Diabetes Sci Technol 2018; 12: 341-348
Quellen:
Diabetes Update 2019
¹ Charleer S et al. Diabetes Obes Metab 2018; 20: 1503-1507
² Christiansen MP et al. Diabetes Technol Ther 2017; 19: 446-456