RET-Inhibitor überzeugt in Schilddrüse und Lunge
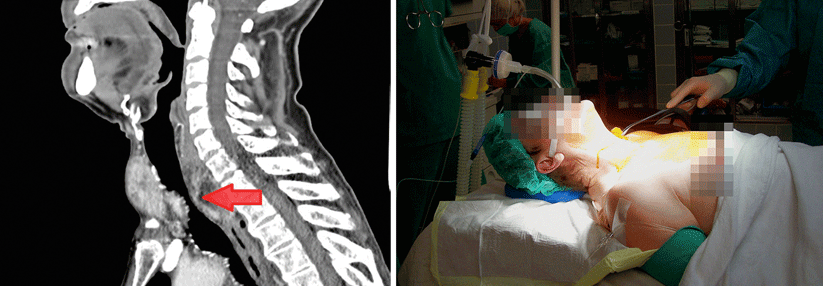
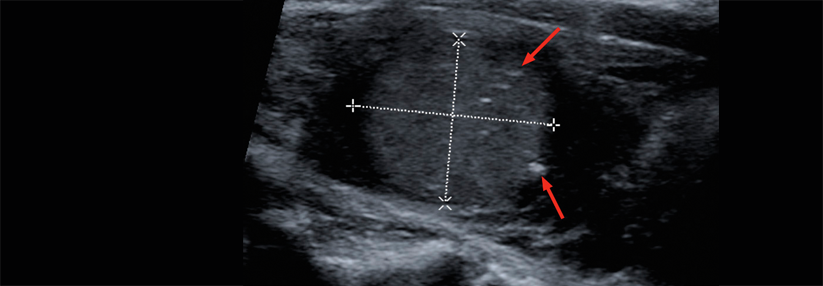 Das medulläre Schilddrüsenkarzinom geht von den C-Zellen aus. Es kommt zu Ablagerungen von Calcitonin (Pfeile).
© wikipedia/Hellerhoff
Das medulläre Schilddrüsenkarzinom geht von den C-Zellen aus. Es kommt zu Ablagerungen von Calcitonin (Pfeile).
© wikipedia/Hellerhoff
Schilddrüse
Eine besondere Rolle spielen RET-Mutationen beim medullären Schilddrüsenkarzinom. 25 % dieser Karzinome treten im Rahmen von einem hereditären Syndrom multipler endokriner Neoplasien (MEN2A und MEN2B) auf, denen eine RET-Mutation in der Keimbahn zugrunde liegt. Aber auch bei den sporadischen Formen weisen etwa 60 % eine somatische RET-Mutation auf. Multikinase-Hemmer wie Vandetanib oder Cabozantinib inhibieren unter anderem RET und wurden bereits beim medullären Schilddrüsenkarzinom eingesetzt. Die Response auf diese Inhibitoren schwankte zwischen 12 % und 65 %. Zudem führten Toxizitäten zu Dosisreduktion und Therapieabbruch.
RET als onkogener Treiber
NSCLC
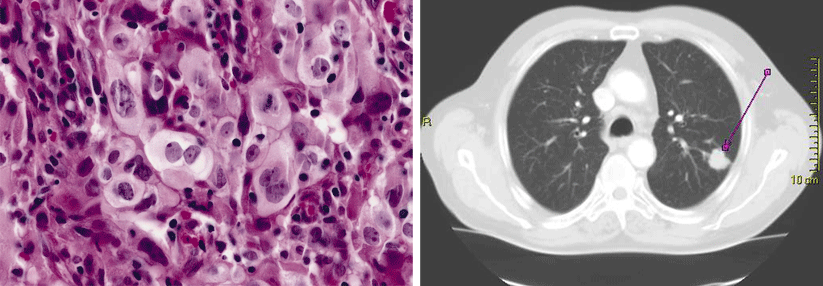
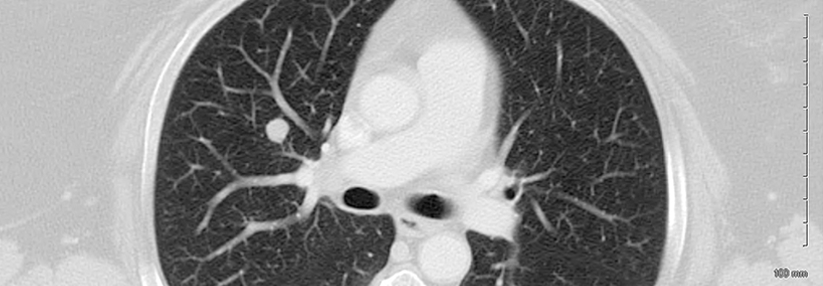
Wesentlich seltener findet man RET-Veränderungen im nicht-kleinzelligen Lungenkarzinom (NSCLC), nur 1–2 % der Betroffenen haben eine RET-Fusion. In der Studie LIBRETTO 001 erhielten 144 Patienten mit RET-fusionspositivem NSCLC zwei Mal täglich 160 mg Selpercatinib, wie Dr. Alexander Drilon vom Memorial Sloan Kettering Cancer Center in New York und seine Kollegen schreiben. Von den Teilnehmern wiesen 36 % zu Anfang Hirnmetastasen auf. Der RET-Inhibitor soll ZNS-gängig sein. Von 105 stark vorbehandelten Menschen, die mindestens eine platinbasierte Chemotherapie erhalten hatten, sprachen 64 % auf die Therapie an (2 % Komplettremissionen). Die Response-Dauer belief sich im Mittel auf 17,5 Monate. Die Ansprechrate der 39 Therapienaiven betrug 85 %. Nach sechs Monaten hielt sie noch bei 90 % an. Auch Patienten mit Hirnmetastasen profitierten von der Behandlung – zehn von elf Erkrankten zeigten einen Rückgang der intrakraniellen Metastasen. Autoren bewerten Toxizität als „niedriggradig“ Die häufigste Nebenwirkung von mindestens Grad 3 war in beiden Studien Bluthochdruck (21 % bzw. 14 %). Weiterhin traten öfter Leberwerterhöhungen und Hyponatriämien auf. Beim Schilddrüsenkarzinom kam es zudem zu Diarrhö und beim NSCLC zu Lymphopenien. Die Rate an Studienabbrüchen aufgrund von Nebenwirkungen lag in beiden Studien bei maximal 2 %. Die fünf bzw. sechs aufgetretenen Todesfälle führten die jeweiligen Autoren nicht auf das Prüfmedikament zurück. Die meisten Menschen mit RET-verändertem Schilddrüsen- oder Lungenkarzinom können somit anhaltend von Selpercatinib profitieren – bei gleichzeitig „niedriggradiger Toxizität“, wie die Forscher schreiben. Und das unabhängig von vorherigen Behandlungen. Ein genetisches Screening könnte – wie bei anderen genetischen Veränderungen von Tumorzellen – helfen, diese Patienten in Zukunft gezielter zu behandeln.Quellen:
1. Wirth LJ et al. N Engl J Med 2020; DOI: 10.1056/NEJMoa2005651
2. Drilon A et al. N Engl J Med 2020; DOI: 10.1056/NEJMdo005846
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).