Subkutaner CD38-Antikörper eignet sich für Patienten mit rezidiviertem Multiplem Myelom
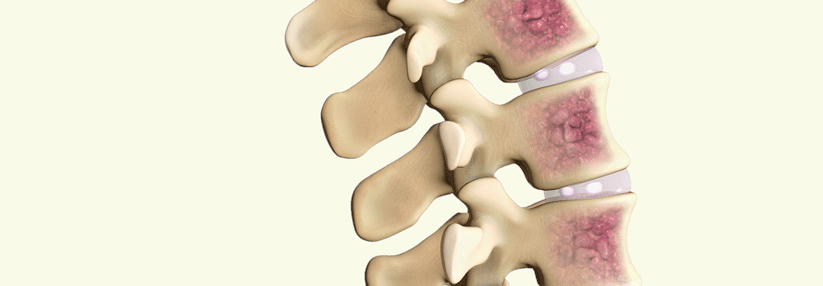
 Die Wirkung des Antikörpers ist unabhängig von Vortherapien des Malignen Myeloms sowie dem zytogenetischem Risiko.
© wikimedia/www.scientificanimations.com (CC BY-SA 4.0)
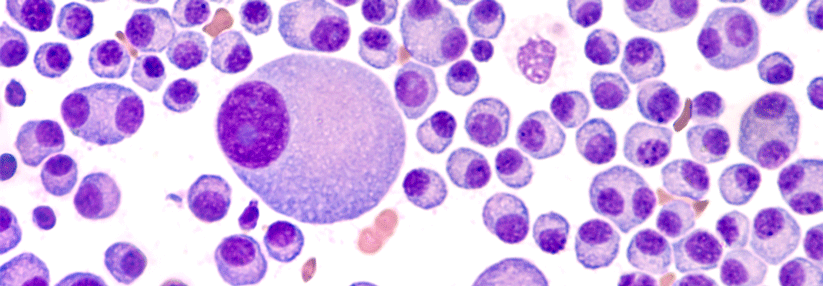
Die Wirkung des Antikörpers ist unabhängig von Vortherapien des Malignen Myeloms sowie dem zytogenetischem Risiko.
© wikimedia/www.scientificanimations.com (CC BY-SA 4.0)
Der gegen das CD38-Oberflächenmolekül gerichtete Antikörper Daratumumab hat in mehreren Studien sowohl beim refraktären Multiplen Myelom (rrMM) als auch bei nicht-transplantationsfähigen und transplantationsfähigen Patienten mit neu diagnostiziertem Multiplem Myelom eine hohe Wirksamkeit gezeigt. Er verlängerte das progressionsfreie (PFS) und das Gesamtüberleben (OS). Mittlerweile steht die s.c.-Formulierung zur Verfügung, die ebenso effektiv sei wie der i.v. applizierte Antikörper und innerhalb von nur fünf Minuten injiziert wird. Das Vorgehen verursacht zudem weniger Injektionsreaktionen, erinnerte Professor Dr. Meletios Dimopoulos von der National and Kapodistrian University of Athens.
In der Phase-3-Studie APOLLO wurde Daratumumab s.c. bei vorbehandelten rrMM-Patienten plus Pomalidomid/Dexamethason (Pd) mit alleinigem Pd-Regime verglichen. In beiden Armen wurden die Therapien bis zum Progress oder bis zu intolerablen Toxizitäten verabreicht. Bei den Teilnehmern handelte es sich laut Prof. Dimopoulos um ein typisches Kollektiv älterer MM-Patienten: Rund 60 % waren über 65 Jahre alt, knapp 20 % über 75 Jahre und etwa ein Drittel hatte ein hohes zytogenetisches Risiko.
Die Erkrankten hatten bereits median zwei Vorbehandlungen erhalten, darunter Lenalidomid und einen Proteasom-Inhibitor. Knapp 80 % waren refraktär gegenüber Lenalidomid, etwa 50 % gegenüber einem Proteasom-Inhibitor und 40 % gegen beides. Die Therapiedauer im Prüfarm fiel mit 11,5 Monaten nahezu doppelt so lang aus wie im Kontrollarm mit 6,6 Monaten.
Ein klinisch relevanter Unterschied von 37 %
Beim PFS als primärem Endpunkt war das Tripleregime dem Duo nach einem medianen Follow-up von 17 Monaten signifikant überlegen: Im Prüfarm überlebten die Patienten im Median 12,4 Monate ohne Progress und damit fast doppelt so lang wie die im Kontrollarm mit median nur 6,9 Monaten. Den Unterschied von 37 % bezeichnete Prof. Dimopoulos als klinisch relevant (Hazard Ratio [HR] für Progression oder Tod 0,63; 95%-KI 0,47–0,85; p = 0,0018). Die Ein-Jahres-Rate des PFS stieg von 35 % auf 52 % in der experimentellen Gruppe. Der Benefit durch Daratumumab wurde konsistent in allen Subgruppen beobachtet und war unabhängig von der Zahl der Vortherapien und zytogenetischem Risiko.
Weiterhin erhöhte das Prüfregime die Ansprechrate gerundet von 46 % auf 69 %, die Rate mindestens kompletter Remissionen von 4 % auf 25 % und die mindestens sehr guter partieller Remissionen von 20 % auf 51 %. Eine Eradikation der minimalen Resterkrankung (MRD) gelang im Kontrollarm bei 2 %, unter Dara-Pd dagegen bei 9 % der Patienten.
Nur wenige Teilnehmer brachen die Behandlung ab
Grad-3/4-Neutropenien und febrile Neutropenien traten unter dem Triplett häufiger auf (68 % vs. 51 % bzw. 9 % vs. 3 %). Zum Therapieabbruch führende Nebenwirkungen waren jedoch selten, ihre Rate in beiden Armen mit 2 % unter Dara-Pd und 3 % unter Pd ähnlich. Auf Basis dieser Daten wertete Prof. Dimopoulos das Triplet als effektives Regime für Patienten nach mindestens einer Vortherapie mit Lenalidomid und einem Proteasom-Inhibitor, das zudem einfacher zu verabreichen und für Patienten angenehmer sei.
Quelle: Dimopoulos MA et al. 62. ASH Annual Meeting (virtuell); Abstract 412
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).