Risikofaktoren Wie die obstruktive Schlafapnoe den Stoffwechsel beeinflusst
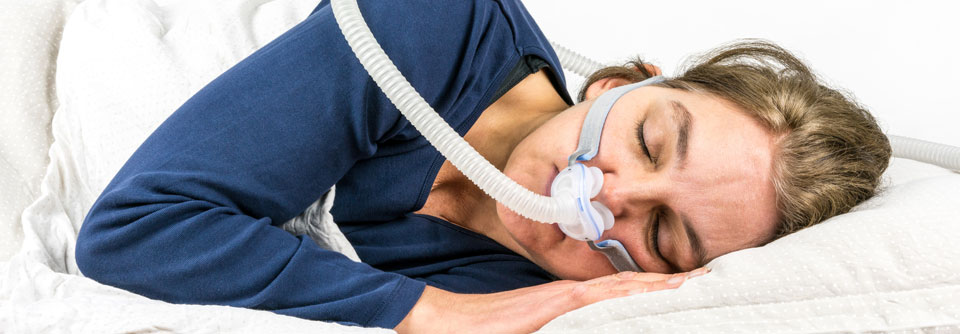
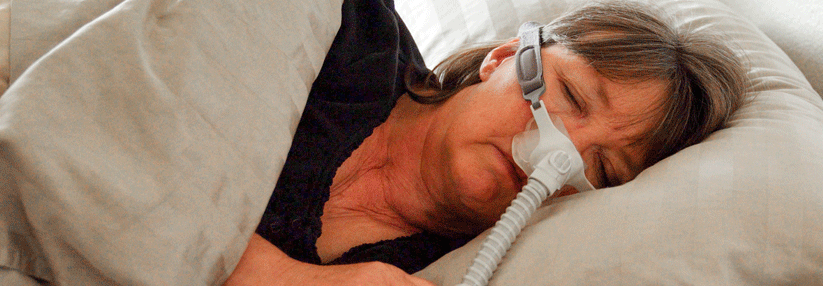
 Regelmäßige Atempausen im Schlaf können spürbar zermürben.
© iStock/NicolasMcComber; iStock/ Elena_Sazanova
Regelmäßige Atempausen im Schlaf können spürbar zermürben.
© iStock/NicolasMcComber; iStock/ Elena_Sazanova
Adipositas erhöht das Risiko für eine obstruktive Schlafapnoe (OSA). Inwiefern nächtliche Atemaussetzer und die damit verbundene schlechte Schlafqualität den Stoffwechsel durcheinander bringen, untersuchte eine Forschungsgruppe um Professor Dr. Babak Mokhlesi, University of Chicago, an 221 Erwachsenen. Diese waren im Schnitt 54,4 Jahre alt und hatten einen BMI von mittleren 35,1 kg/m2.
Die obstruktive Schlafapnoe
Bei einer obstruktiven Schlafapnoe entspannen sich die Muskeln im Kieferbereich zeitweise, sodass die oberen Atemwege kollabieren und dadurch teilweise (Hypopnoe) bzw. komplett (Apnoe) blockiert werden. Die kurzen Atemstillstände führen zu einem vorübergehenden Sauerstoffmangel und CO2-Überschuss im Blut, zu Beinaheerwachen, Schlaffragmentierung, erhöhtem oxidativem Stress und Inflammation.
Ein wahrnehmbares Zeichen für die obstruktive Schlafapnoe ist lautes Schnarchen. Patienten berichten weiterhin über exzessive Tagesmüdigkeit, Erstickungsgefühle, trockenen Mund oder Halsschmerzen, morgendliche Kopfschmerzen, Konzentrationsschwierigkeiten während des Tages, Stimmungsschwankungen, nächtliches Schwitzen und verminderte Libido. Als Therapiegoldstandard gilt die Anwendung eines CPAP-Atemgeräts, das den Luftdruck auf die Atemwege erhöht und sie dadurch im Schlaf offen hält. Eine weitere Option ist eine Zahnschiene, die den Unterkiefer im Schlaf nach vorne schiebt.
Die Fragestellung des Teams: Gehen eine verminderte Schlafdauer sowie die Schwere der OSA bei Menschen mit Prädiabetes bzw. frisch diagnostiziertem Typ-2-Diabetes mit einer verringerten Insulinempfindlichkeit und reduzierten Betazellantwort auf Glukose einher? Dafür hatte man die Schlafqualität per Aktigraphie und im Schlaflabor ermittelt. Die Teilnehmenden trugen für jeweils eine Woche einen Aktivitätsmesser am Handgelenk, der Ruhe- und Schlafzyklen sowie Aktivität aufzeichnete. Außerdem unterzogen sie sich für eine Nacht einer Polysomnographie. Die Insulinempfindlichkeit hatte man mit einem oralen Glukosetoleranztest (oGTT) und einem zweistufigen Insulin-Clamp untersucht. Die Probanden schliefen im Schnitt 6,6 Stunden pro Nacht. Bei 89 % von ihnen wurde eine OSA festgestellt, die mithilfe eines Apnoe-Hypopnoe-Index (AHI) als fünf oder mehr Atemstillstände pro Stunde definiert wurde. Rund 20 % der Teilnehmenden wiesen eine leichte, 28 % eine mittelschwere und 41 % eine schwere OSA auf. Diese korrelierten signifikant mit dem Glukosestoffwechsel: Ein um 40 Punkte erhöhter AHI war mit einem um 0,12 Prozentpunkte höheren HbA1c-Wert assoziiert. Allerdings gingen weder hohe AHI noch eine verkürzte Schlafdauer mit erhöhten Nüchternwerten bzw. 2-Stunden-Werten beim oGTT oder mit einer verringerten Insulinempfindlichkeit bzw. Betazellantwort einher.
Was auf den ersten Blick verwundert, erklären die Studienautoren damit, dass in früheren Untersuchungen zwar ein Zusammenhang zwischen gestörter Insulinempfindlichkeit und Schlafmangel festgestellt wurde. Allerdings seien darin gesunde Personen anstelle von übergewichtigen bzw. adipösen Menschen mit Prädiabetes eingeschlossen gewesen. Zudem hatte man damals weder Schlafgewohnheiten noch körperliche Aktivität objektiv gemessen.
Die Forschenden vermuten, dass der fehlende Zusammenhang zwischen OSA/Schlafmangel und Insulinempfindlichkeit/Betazellantwort an der hohen Prävalenz von Adipositas in ihrem Kollektiv lag. Möglicherweise sei der Einfluss der Adipositas ab einer bestimmten Schwelle so stark, dass der Effekt von OSA und Schlafmangel auf Insulinresistenz und Betazelldysfunktion weniger relevant ist. Weitere Studien, besonders an nicht-adipösen Patienten mit Prädiabetes, seien erforderlich um herauszufinden, ob eine OSA-Therapie oder längere Schlafdauer sich bei ihnen positiv auf Insulinempfindlichkeit und Betazellantwort auswirken und damit das Risiko für einen Typ-2-Diabetes verringern können.
Quelle: Mokhlesi B et al. Diabetes Care 2021; 44: 993-1001; DOI: 10.2337/dc20-2127