Myokard-Versteifung aufhalten
 Im Falle der AA-Amyloidose im Rahmen autoimmuner Erkrankungen gilt es, die chronisch-entzündliche Grunderkrankung zu kontrollieren.
© dima_oris – stock.adobe.com
Im Falle der AA-Amyloidose im Rahmen autoimmuner Erkrankungen gilt es, die chronisch-entzündliche Grunderkrankung zu kontrollieren.
© dima_oris – stock.adobe.com
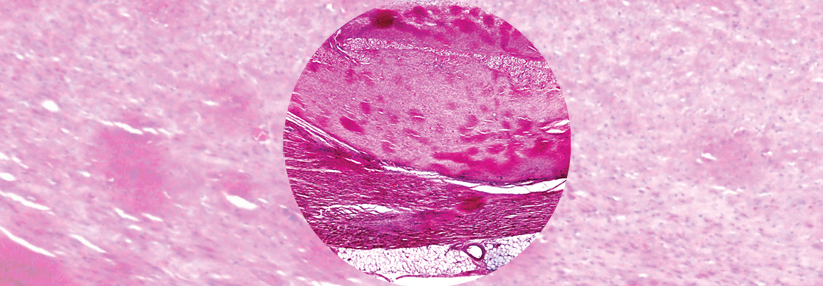
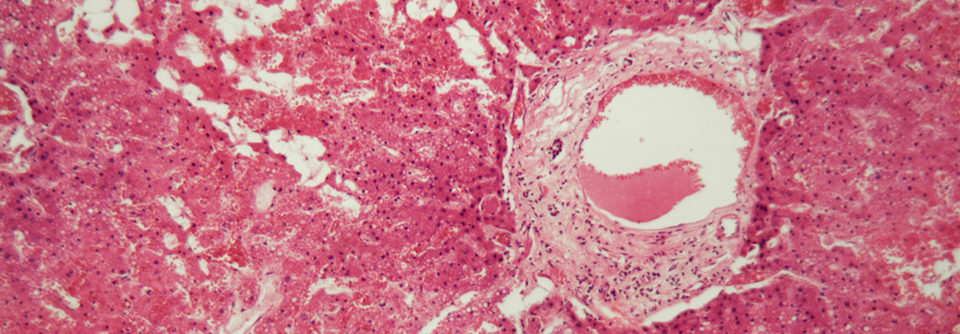
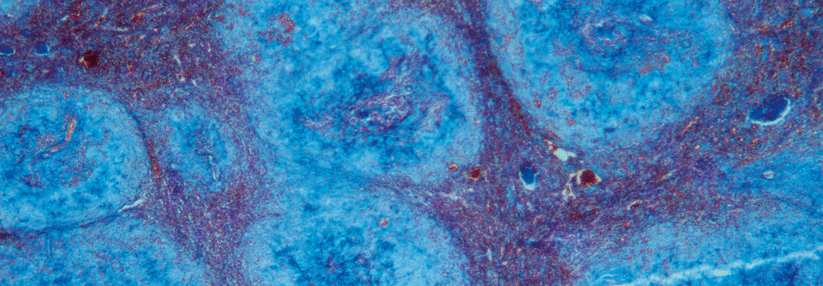
Eine Amyloidose entsteht durch fehlgefaltete Proteine. Diese reihen sich aneinander und bilden Amyloidfibrillen, die sich ubiquitär im Körper ablagern. Je nach betroffenem Organ entwickeln sich verschiedene Beschwerden (siehe Kasten). Mit einer kardialen Beteiligung gehen typischerweise vier Amyloidoseformen einher:
- Die Leichtketten-Amyloidose (AL-Amyloidose) beruht auf einer primär nicht-malignen monoklonalen Gammopathie oder tritt im Rahmen vom Multiplen Myleom, Lymphomen oder dem Morbus Waldenström auf.
- Bei der Transthyretin-Amyloidose (ATTR-Amyloidose) wird fehlgefaltetes Transthyretin (TT) abgelagert. Im Falle der genetisch bedingten, vererbten Form (ATTRv) handelt es sich um instabiles TT, beim Wildtyp (ATTRwt) um reguläres TT. Die ATTRwt betrifft primär das Herz und manifestiert sich häufig erst im späteren Lebensalter. Die vererbte Form beginnt oft schon im Jugendalter, wobei Herz und Nerven unterschiedlich stark betroffen sind.
- Die AA-Amyloidose ist eine eher seltene Komplikation entzündlich-rheumatischer oder autoimmuner Erkrankungen. Abgelagert werden Akute-Phase-Proteine, bei jedem zehnten Betroffenen liegt eine kardiale Beteiligung vor.
- Eine Punktmutation ist Ursache der Apolipoprotein-Amyloidose. Hierbei lagern sich die Proteine vor allem in der Niere, aber auch im Herz ab.
Allen kardialen Amyloidosen ist gemeinsam, dass sie häufig erst spät diagnostiziert werden, betonen PD Dr. Carolin Morbach von der Universitätsklinik Würzburg und Kollegen. Dabei ist eine frühzeitige Diagnose essenziell, um eine kausale Therapie einleiten zu können und so die Prognose der Patienten zu verbessern.
Intrazelluläre Ablagerungen versteifen das Myokard
Der Verdacht auf eine kardiale Amyloidose entsteht durch klinische Symptome, aufgrund eines (Zufalls-)Befundes in der Echokardiografie oder weil im Rahmen einer Amyloidose danach gesucht wird. Klinisch bemerkbar machen sich die interzellulären Ablagerungen durch eine erhöhte Steifigkeit des Myokards. Dies führt zu einer Herzinsuffizienz mit Belastungsdyspnoe, Ödemen und Nykturie. Im Herzecho fallen verdickte Ventrikelwände und Herzklappen auf, die Bewegungsanalyse des Myokards zeigt eine Störung der Kontraktilität unter Aussparung der apikalen Segmente (sog. Apical Sparing).
Bei Verdacht auf eine kardiale Amyloidose steht laut Dr. Morbach ein Test auf Leichtketten an erster Stelle im diagnostischen Algorithmus. Ihr Nachweis erfolgt in Serum und Urin mit Elektrophorese und Immunfixation. Werden Leichtketten gefunden, ist die Diagnose durch Biopsie eines betroffenen Organs histologisch zu bestätigen. Bei Vorliegen einer AL-Amyloidose muss der Patient umgehend hämatologisch-onkologisch mitbetreut werden.
| Typische Symptome und Begleitbefunde der Amyloidose | |
|---|---|
| Kardial | |
| Herzinsuffizienz
Störungen des Reizleitungssystems
| |
| Extrakardial | |
| Niere
Magen-Darm-Trakt
Augen
Weichteile
| Muskuloskelettal
Gefäße
Nervensystem
|
In manchen Fällen ist eine Myokardbiopsie notwendig
Sind keine Leichtketten nachweisbar und eine AA-Amyloidose durch normwertige Serum-Amyloid-A-Spiegel ausgeschlossen, ist nach einer ATTR-Amyloidose zu fahnden. Dies geschieht mithilfe der Skelettszintigrafie. In einigen Fällen, wie einem typischen klinischen Bild mit negativen Befunden in der Bildgebung, sollte die Diagnose kardiale Amyloidose durch weitere Schritte bis hin zur Myokardbiopsie ausgeschlossen bzw. erhärtet werden.
Die Therapie der Herzinsuffizienz bei kardialer Amyloidose zeigt einige Besonderheiten. So entwickeln die Patienten bei Volumenbelastung schnell eine Dyspnoe und ein Lungenödem. Sie müssen sich deshalb strikt an die empfohlene Trinkmenge von 1,5 Liter pro Tag halten. Essenziell ist zudem eine dauerhafte, forcierte Diurese.
Aufgrund der restriktiven Störung ist das erkrankte Herz nicht in der Lage, bei vermehrter Belastung sein Schlagvolumen wesentlich zu steigern. Stattdessen erhöht es die Frequenz. Betablocker können daher die Belastungsfähigkeit der Betroffenen empfindlich einschränken. Zeigen sich solche Beschwerden, ist das Absetzen oder eine Dosisreduktion der Substanzen zu erwägen.
Eine Neigung zu Hypotonie ermahnt zu Vorsicht beim Einsatz von ACE-Inhibitoren und der Kombination Sacubitril/Valsartan. Laut Autoren wurden für die genannten Substanzklassen bisher keine Prognoseverbesserung bei kardialer Amyloidose nachgewiesen, sie sollten daher bei fehlender Toleranz abgesetzt werden. Hilfreich sind dagegen das Tragen von Stützstrümpfen und eventuell die Gabe von Midodrin.
Neben der Behandlung der Herzinsuffizienz steht bei den beiden häufigeren Formen der kardialen Amyloidose die kausale Therapie im Mittelpunkt. Bei der AL-Amyloidose erfolgt je nach Entität und Allgemeinzustand des Patienten die individuell maßgeschneiderte Therapie, z.B. mit Hochdosis-Chemotherapie bzw. autologer Stammzelltransplantation.
Zur Behandlung der ATTR-Amyloidose ist der Wirkstoff Tafamidis zugelassen. Er stabilisiert Transthyretin, bremst damit das Fortschreiten der Erkrankung und zeigt positive Effekte auf Mortalität und Morbidität. Aufgrund der hohen Therapiekosten empfehlen Dr. Morbach und Kollegen allerdings, den therapeutischen Nutzen regelmäßig zu evaluieren.
Für die beiden anderen Formen der kardialen Amyloidose gibt es keine kausale Therapie. Im Falle der AA-Amyloidose im Rahmen autoimmuner Erkrankungen gilt es, die chronisch-entzündliche Grunderkrankung zu kontrollieren. Ist eine solche nicht eruierbar, kann auf Basis von Fallberichten eine Antikörpertherapie erwogen werden, z.B. mit Tocilizumab.
Quelle: Morbach C et al. Dtsch Med Wochenschr 2022; 147: 1522-1529; DOI: 10.1055/a-1810-9199
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).