Amyloidose: Anti-CD38-Antikörper zusätzlich zur Immunchemotherapie verzögert Progress
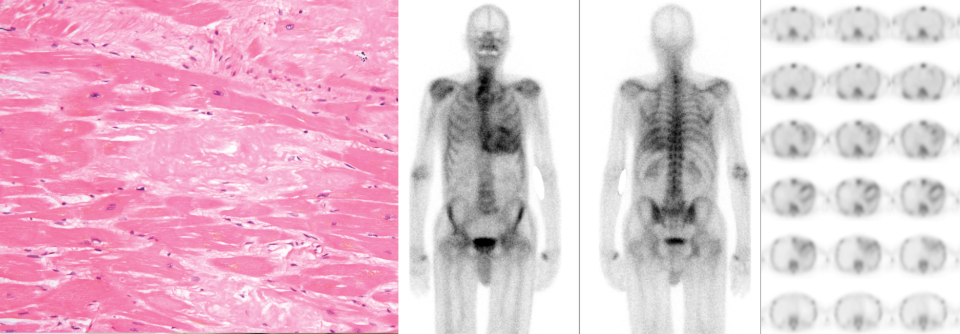
 Bei der Amyloidose bilden sich Amyloidablagerungen in verschiedenen Organen, wie hier im Herzen.
© Science Photo Library/Biophoto Associates
Bei der Amyloidose bilden sich Amyloidablagerungen in verschiedenen Organen, wie hier im Herzen.
© Science Photo Library/Biophoto Associates
Ein wichtiges Therapieziel bei der neu diagnostizierten systemischen Leichtketten(AL)-Amyloidose ist ein schnelles, tiefes und anhaltendes hämatologisches Ansprechen. So soll die fortschreitende amyloidvermittelte Schädigung der Organfunktionen, insbesondere des Herzens, verlangsamt und das Überleben verbessert werden. Aktuell sterben etwa 30 % der Patienten bereits im ersten Jahr – wirksamere Therapien werden deshalb dringend benötigt, betonte Professor Dr. Efstathios Kastritis, Universität Athen.
In einer Phase-2-Studie war eine Monotherapie mit dem Anti-CD38-Antikörper Daratumumab bei rezidivierter/refraktärer AL-Amyloidose mit einem tiefen und anhaltenden hämatologischen Ansprechen assoziiert.1 In der randomisierten und offenen ANDROMEDA-Studie wurden daraufhin Effektivität und Sicherheit von Daratumumab subkutan zusätzlich zu Cyclophosphamid, Bortezomib und Dexamethason (CyBorD) mit CyBorD allein verglichen.2
Das Studiendesign
Tieferes und schnelleres Ansprechen mit Daratumumab
Bei zwei Drittel der Patienten waren mindestens zwei Organe von der Amyloidose betroffen, bei über 70 % das Herz, bei 59 % die Niere. Das kardiale Mayo-Stadium* lag bei mehr als einem Drittel der Patienten bei IIIA und IIIB, betonte Prof. Kastritis. Zur Auswertung nach median 11,4 Monaten erhielten noch 72 % der Personen im Prüfarm die geplante Daratumumab-Monotherapie. Im Kontrollarm hatten bereits 42 % eine Folgetherapie erhalten, die meist aus Daratumumab oder einer Stammzelltransplantation bestand. Das Ansprechen war durch die Antikörpergabe tiefer und es wurde schneller erzielt: Ein hämatologisches Komplettansprechen (CR) als primären Endpunkt erreichten 53 % (vs. 18 %). Damit erhöhte Daratumumab die Wahrscheinlichkeit eines hämatologischen CR um das Fünffache (Odds Ratio 5,1; 95%-KI 3,2–8,2; p < 0,0001). Auch beim Ansprechen nach sechs Monaten zeigte sich mit 50 % CR unter Daratumumab und 14 % in der Kontrolle ein ähnlicher Vorteil (OR 6,1; p > 0,0001). Das hämatologische CR trat im Prüfarm nach median 60 Tagen ein, mit der Standardtherapie erst nach 85 Tagen. Der Vorteil für die Daratumumab-Kombination hinsichtlich des hämatologischen CR fand sich in fast allen Subgruppen, auch bei fortgeschrittener Herzinsuffizienz. Zudem war der Anteil von Patienten, die mindestens ein sehr gutes partielles Ansprechen (VGPR) erzielten, signifikant höher (79 % vs. 49 %; OR 3,8; p < 0,0001) und das Ansprechen wurde schneller erreicht (17 Tage vs. 25 Tage). Das bessere hämatologische Ansprechen schlug sich in einer stabileren Organfunktion nieder. Die Wahrscheinlichkeit für eine deutliche Verschlechterung der Organfunktion, definiert als hämatologischer Progress, kardiale oder Nierenerkrankung im Endstadium bzw. Tod, war um 42 % verringert (HR 0,58; p = 0,023). Der Median des Überlebens ohne solch ein Ereignis oder eine Folgetherapie war mit Daratumumab-CyBorD noch nicht erreicht und lag mit CyBorD bei 10,4 Monaten (HR 0,40; p > 0,0001). Das Ansprechen der betroffenen Organe nach sechs Monaten verdoppelte Daratumumab ungefähr: Das Herz sprach bei 42 % der Patienten an (vs. 22 %), die Niere bei 54 % (vs. 27 %).Gesamtüberlebensdaten lassen noch auf sich warten
Die Hinzunahme des Antikörpers führte zu etwas mehr Infektionen, die Therapieabbruchrate war aber in beiden Armen ähnlich, so der Experte. Ergebnisse zum Gesamtüberleben gibt es noch nicht. Für Prof. Kastritis ist Daratumumab plus CyBorD aber schon jetzt ein neuer potenzieller Standard für die systemische AL-Amyloidose.* Erhöhung von TNT und NT-ProBNP
Quellen:
1. Roussel M et al. Blood 2020; 135: 1531-1540; DOI: 10.1182/blood.2019004369
2. Kastritis E et al. EHA25 Virtual Congress; Abstract LB2604
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).