Wenn es richtig dicke kommt
 ARNI bremsen den Abfall der Nierenfunktion, schützen vor Klinikeinweisungen wegen Herzinsuffizienz und verhindern kardiovaskuläre Todesfälle.
© natali_mis – stock.adobe.com
ARNI bremsen den Abfall der Nierenfunktion, schützen vor Klinikeinweisungen wegen Herzinsuffizienz und verhindern kardiovaskuläre Todesfälle.
© natali_mis – stock.adobe.com
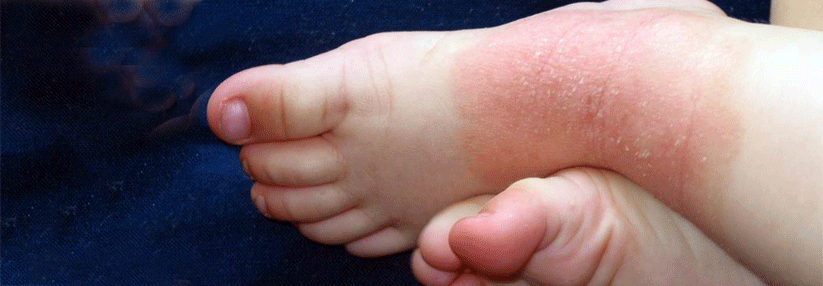
Ist das Zusammenspiel von Herz, Nieren und Stoffwechsel beeinträchtigt, steigt insbesondere das Risiko für kardiovaskuläre Erkrankungen. Meist liegen der Störung Übergewicht und die damit einhergehenden negativen Effekte des dysfunktionalen Fettgewebes zugrunde, erläutern Prof. Dr. Chiadi Ndumele von der Johns Hopkins University in Baltimore und Koautoren. Kommt es im Zuge des Krankheitsgeschehens zur manifesten Multiorganerkrankung mit Diabetes mellitus Typ 2, chronischem Nierenleiden und Herz-Kreislauf-Erkrankung, spricht man vom cardiovascular-kidney-metabolic syndrome (auf Deutsch etwa: kardiovaskuläres Nieren-Stoffwechsel-Syndrom).
Stadium richtet sich nach den Risikofaktoren
Als Experten der American Heart Association (AHA) erläutern die Kollegen die Einteilung des Syndroms in verschiedene Stadien und erklärt, welche Therapie jeweils infrage kommt. Unterschieden werden vier Phasen:
- Im Stadium 0 liegen keine Risikofaktoren für das Syndrom vor.
- Patienten im Stadium 1 haben Übergewicht (BMI > 25) und ein Übermaß an abdominalem Fettgewebe, bei möglicherweise gestörter Glukosetoleranz oder Prädiabetes.
- Das Stadium 2 ist durch Hypertonie und Stoffwechselerkrankungen gekennzeichnet, etwa Hypertriglyzeridämie, Diabetes oder metabolisches Syndrom, eventuell eine chronische Nierenerkrankung mit moderatem Risiko.
- Im Stadium 3 liegt zusammen mit Adipositas eine subklinische kardiovaskuläre Erkrankung oder Ähnliches vor, z.B. ein hohes kardiovaskuläres Risiko oder ein hochriskantes Nierenleiden.
- Im Stadium 4 findet sich im Rahmen des Syndroms eine manifeste kardiovaskuläre Krankheit. Zusätzlich fallen Faktoren auf, die die Progression des kardiovaskulären Nieren-Stoffwechsel-Syndroms beschleunigen.
Die Behandlung richtet sich nach der Krankheitsphase: Im Stadium 0 steht der Erhalt der kardiovaskulären Gesundheit im Vordergrund, wozu auch das Vermeiden einer Gewichtszunahme gehört. Im Stadium 1 geht es darum, metabolische Risikofaktoren zu minimieren. Häufig reichen der Umstieg auf eine herzgesunde Ernährung plus eine angemessene Bewegung schon aus. Bereits eine Gewichtsabnahme um ≥ 5 % bringt signifikante Effekte für Blutdruck, Blutzucker und Fettwerte, eine Reduktion um ≥ 10 % verhindert kardiale Ereignisse. Eine medikamentöse Adipositastherapie und bariatrische Operationen können die Behandlung ergänzen.
Im Stadium 2 sollen weitere kardiovaskuläre Erkrankungen verhindert werden. Wie das geschieht, hängt von der jeweiligen Situation ab. So kann eine Reduktion der Hypertonie multiplen Gefäßereignissen vorbeugen. In den Leitlinien wird generell zum Zielwert von 130/80 mmHg geraten. Eine Pharmakotherapie in Ergänzung zu einem gesunden Lebensstil ist empfehlenswert für Menschen ≥ 65 Jahre, bei Diabetes und bei einem Zehn-Jahres-Risiko für arteriosklerotische kardiovaskuläre Erkrankungen (ASCVD) ≥ 10 %. Liegen Diabetes, Albuminurie oder andere chronische Nierenleiden vor, plädieren die Autoren für die bevorzugte Gabe von ACE-Hemmern und AT1-Rezeptorantagonisten, um die renale Progression aufzuhalten.
Triglyzeride in den Normbereich bringen
Auch zwischen ASCVD und Hypertriglyzeridämie besteht ein Kausalzusammenhang, betonen die Autoren. Wenn Lebensstilmodifikationen allein nicht ausreichen, lassen sich die Blutfettwerte mit Statinen zumindest moderat reduzieren. Oberhalb von 500 mg/dl sind Fibrate indiziert.
Bei Diabetes und dem damit einhergehenden ASCVD-Risiko ist eine konsequente Statintherapie angezeigt. Gegebenenfalls wird sie durch Ezetimib ergänzt. Anzustreben ist eine Reduktion des LDL-Cholesterins um ≥ 50 %. Eine kardioprotektive antiglykämische Therapie mit SGLT2-Inhibitoren und GLP1-Rezeptoragonisten wird für Stoffwechselkranke mit entsprechender Komorbidität empfohlen. SGLT2-Inhibitoren reduzieren auch das Risiko für eine Verschlechterung der Nierenfunktion. GLP1-Analoga ist bei HbA1c-Werten > 9 % oder höherem Insulinbedarf der Vorzug zu geben, da diese Substanzen den Blutzuckerspiegel stärker senken. Wegen der positiven Effekte auf das Körpergewicht eignen sie sich auch zur Behandlung bei schwerer Adipositas (BMI ≥ 35). Besteht ein hohes Herzinsuffizienzrisiko, können SGLT2-Inhibitoren die Wahrscheinlichkeit für Klinikaufenthalte verringern.
Im Fall einer chronischen Nierenerkrankung mit Albuminurie vermindern ACE-Hemmer und AT1-Antagonisten unabhängig vom Vorliegen eines Diabetes den Krankheitsprogress und das kardiovaskuläre Risiko. Auch SGLT2-Inhibitoren können verhindern, dass die renale Erkrankung fortschreitet. Sie wirken zusätzlich kardioprotektiv.
Im Stadium 3 empfehlen die Verfasser schon bei asymptomatischer linksventrikulärer systolischer Dysfunktion eine Behandlung mit ACE-Hemmern und Betablockern. Bei Patienten mit Diabetes senken SGLT2-Inhibitoren das Risiko für eine manifeste Herzinsuffizienz. Die subklinische ASCVD lässt sich anhand von Koronarkalk nachweisen. Patienten mit Punktwerten > 100 tragen ein Zehnjahresrisiko ≥ 7,5 %. In dieser Situation ist die präventive Gabe von ASS sinnvoll.
Im Stadium 4 sollten alle Patienten mit manifester ASCVD zusätzlich zum hochwirksamen Statin ASS oder einen P2Y12-Inhibitor einnehmen. Die Therapie der Herzinsuffizienz hat leitliniengerecht zu erfolgen, worunter die US-amerikanischen Autoren den Einsatz von Betablockern, Angiotensin-Rezeptor-Neprilysin-Inhibitoren (ARNI), Aldosteronrezeptor-Antagonisten und SGLT2-Inhibitoren verstehen. Vor allem bei reduzierter linksventrikulärer Funktion verbessert diese Therapie die Prognose. Bei Adipositas können GLP1-Agonisten das Risiko für Koronarkomplikationen signifikant senken. Liegt eine Kombination von chronischer Nierenerkrankung und KHK vor, werden neben der Statintherapie ACE-Hemmer und AT1-Rezeptorantagonisten empfohlen.
Der Einsatz von SGLT2-Hemmer erfordert eine eGFR > 20 ml/min/1,73 m2. Die Substanzen reduzieren die renale Progression und die KHK-Mortalität, sie verhindern Klinikeinweisungen wegen Herzinsuffizienz sowie schwere kardiale Komplikationen. Finerenon darf bei einer eGFR > 25 ml/min/1,73 m2 verordnet werden und vermindert Nieren- und Herzereignisse. ARNI bremsen den Abfall der Nierenfunktion, schützen vor Klinikeinweisungen wegen Herzinsuffizienz und verhindern kardiovaskuläre Todesfälle.
Quellen:
1. Ndumele CE et al. Circulation 2023; DOI: 10.1161/CIR.0000000000001184
2. Ndumele CE et al. Circulation 2023; DOI: 10.1161/CIR.0000000000001186
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).