Wie Rheuma in die Atemwege beißt
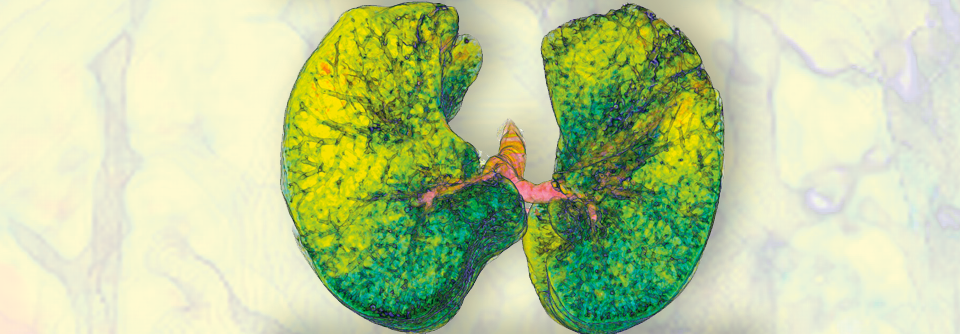 Interstitielle Lungenerkrankung in einer kolorierten 3D-CT-Aufnahme.
© Science Photo Library/Fung, K.H.
Interstitielle Lungenerkrankung in einer kolorierten 3D-CT-Aufnahme.
© Science Photo Library/Fung, K.H.
Bei 60 % der Patienten mit rheumatoider Arthritis (RA) werden die Atemwege in Mitleidenschaft gezogen, schreiben Dr. Suha Kadura und Dr. Ganesh Raghu vom Center for Interstitial Lung Diseases, University of Washington. Am häufigsten trifft es das Parenchym in Form einer interstiellen Lungenerkrankung (ILD). Daneben können aber auch das Cricoarytenoidgelenk, die Bronchien und Bronchioli sowie die Pleura involviert sein.
Mit citrullinierten Proteinen geht's los
Pathophysiologisch liegt der respiratorischen Beteiligung vermutlich eine Kombination aus genetischen Einflüssen, Umweltfaktoren und Autoimmunprozessen zugrunde. Die genetische Veranlagung führt in der Lunge (und in den Gelenken) zu einer Vermehrung citrullinierter Proteine und anschließend zu autoinflammatorischen Reaktionen, bei denen u.a. Zytokine, Antikörper (z.B. ACPA) und Wachstumsfaktoren eine Rolle spielen. Ein wichtiger Mitspieler ist Interleukin-17, das wie andere TH-17-Zytokine direkte Effekte auf Fibroblasten hat. In der Folge werden diese stimuliert und extrazelluläre Matrix produziert, was in der Lunge zur RA-ILD und Fibrose, in den Gelenken zu rheumatischen Veränderungen führt.
Wo die initiale Zündung passiert, wird noch diskutiert. Eine Theorie besagt, dass die durch autoimmune Prozesse in der Synovia entstehenden Antikörper mit ähnlichen Antigenen in der Lunge kreuzreagieren, die pulmonale Erkrankung also vom Gelenk ausgeht. Hierzu passt, dass die meisten Lungenbeteiligungen bei RA nach den Gelenkbeschwerden auftauchen. Die Mukosatheorie postuliert es gerade andersherum: Danach startet der autoimmune Prozess in der Mukosa von Magen-Darm-Trakt oder Atemwegen und schlägt erst dann auf die Gelenke. Unterstützt wird diese Theorie durch einige neue Untersuchungen. So fand man beispielsweise bei Menschen mit RA-Risiko IgA-ACPA im Sputum und bei Patienten mit früher rheumatoider Arthris ACPA in der bronchoalveolären Lavage.
| Mit der rheumatoiden Arthritis assoziierte Lungenerkrankungen (Auswahl) | ||
|---|---|---|
| Phänotyp | Häufigkeit | Merkmale |
| ILD mit UIP-Muster | bis zu 66 % | Veränderungen zeigen sich vor allem im basalen und subpleuralen Bereich. Typisch sind retikuläre Zeichnungen sowie ein Honigwabenmuster, oft kommt es zu Traktionsbronchiektasen. Milchglastrübungen kommen im Gegensatz zum NSIP-Muster selten vor. |
| ILD mit NSIP-Muster | bis zu 57 % | Als typisch gelten ausgeprägte, meist bilateral verteilte Milchglastrübungen. Traktionsbronchiektasen und subpleurale Aussparungen kommen vor. |
| organisierende Pneumonie | bis zu 11 % | Erkennbar sind lokale, z.T. von ringförmigen Konsolidierungen umgebene Milchglastrübungen (umgekehrtes Halo-Zeichen). |
| andere, z.B. lymphozytäre (LIP) oder desquamative interstitielle Pneumonie (DIP) | selten | Veränderungen finden sich oft in den oberen Lungenlappen: Milchglastrübungen und dünnwandige Zysten, bei der DIP alveoläre Makrophagen-Ansammlungen, bei der LIP kleine Lymphozyten und Plasmazellen in Alveolen und Alveolarsepten. |
| Rheumaknötchen | < 1 % radiologisch, häufiger in Autopsien | Charakteristisch sind meist asymptomatische, einzeln oder multipel auftretende, an Rundherde erinnernde Knötchen. Bei Ruptur drohen Infektion, Pleuraerguss oder Fisteln. |
| Cricoarytenoiditis | bis zu 75 % | Die Arthritis des Gelenks zwischen Stell- und Ringknorpel führt zu anhaltenden Stimmveränderungen mit Heiserkeit und Stridor. |
| Bronchiektasen | ca. 30 % in der HRCT | Oft fehlen klinische Zeichen, manchmal sind die Bronchiektasen mit chronischen Infektionen verbunden. |
| Pleuraerguss | 3–5 % | Betroffen sind vor allem Männer mittleren Alters mit positivem RF und Rheumaknoten. Der Erguss ist meist steril mit einem pH < 7,3, Glukose < 60 mg/dl und erhöhtem LDH. |
| Bronchiolitis | bis zu 30 % | Betroffen sind vor allem Frauen mit hohen Rheumafaktortitern und langer Erkrankungsdauer. |
| nach Kadura S, Raghu G. Eur Respir Rev 2021; 30: 210011; doi: 10.1183/16000617.0011-2021 | ||
An erster Stelle in der Diagnostik einer RA-assoziierten Lungenerkrankung steht die Routine-Thoraxaufnahme. Um aber das Muster zu erkennen und Differenzialdiagnosen (Medikamentennebenwirkungen, Pneumokoniosen, andere Bindegewebserkrankungen oder iatrogene Ursachen) auszuschließen, kann man auf eine hochauflösende CT-Aufnahme (HRCT) nicht verzichten. Die Beurteilung der Aufnahmen ist diffizil und erfordert die enge Zusammenarbeit zwischen Radiologen, Rheumatologen und Pneumologen.
Lungenbiopsie selten erforderlich
Die bronchoalveoläre Lavage (BAL) hilft dagegen diagnostisch wenig. Sie ergibt bei einer RA-ILD zwar oft auffällige, aber unspezifische Befunde. Am ehesten wird die BAL dazu genutzt, um Infektionen auszuschließen. Auch die Lungenbiopsie kommt eher selten in Betracht. Zwar kann man damit das radiologisch diagnostizierte Muster bestätigen. Dieser Nutzen überwiegt jedoch in den seltensten Fällen das Risiko des invasiven Verfahrens, schreiben die Autoren. Erwogen werden sollte die Lungenbiopsie, wenn sich in der HRCT kein deutliches UIP(usual interstitial pneumonia)-Muster erkennen lässt, die Lungensymptome vor den Gelenkbeschwerden auftreten oder um Differenzialdiagnosen auszuschließen.
Ob eine RA-assoziierte Lungenerkrankung der Therapie bedarf, hängt von ihrer Schwere und dem Fortschreiten ab. Deshalb müssen nicht nur bei der Basisuntersuchung, sondern auch regelmäßig im Verlauf HRCT und Lungenfunktionstests durchgeführt werden. Für die Therapieentscheidung zählen zudem Alter, Komorbiditäten und Befallsmuster. Leider gibt es bisher noch keine randomisierten kontrollierten Studien, die eine evidenzbasierte Behandlung ermöglichen.
Auf Basis der pathogenetischen Vorgänge stehen verschiedene therapeutische Ansätze zur Verfügung. Vor allem in Fällen einer ILD-NSIP (nonspecific interstitial pneumonia) oder der organisierenden Pneumonie kommen Steroide zum Einsatz. Sie führen radiologisch und klinisch zu einer Verbesserung. Auch bei 50 % von 84 RA-UIP-Patienten konnten Glukokortikoide allein oder in Kombination mit Immunsuppressiva in einer Studie die Erkrankung stabilisieren oder verbessern, wobei sich allerdings im Vergleich mit der unbehandelten Kontrollgruppe kein signifikanter Unterschied im Überleben ergab. In einer weiteren Studie profitierte die Untergruppe von elf RA-ILD-Patienten von der Gabe von Kortison hinsichtlich forcierter Vitalkapazität (FVC), Gehtestparametern und subjektiver Einschätzung.
Die antiproliferativen bzw. zytotoxischen Wirkstoffe Cyclophosphamid und Mycophenolat-Mofetil (MMF) zeigten unterschiedliche Erfolge. In einer retrospektiven Studie mit 21 RA-ILD-UIP-Patienten war die mittlere Überlebenszeit der Patienten mit Cyclophosphamid besser als ohne. Nachteil der Behandlung: die ausgeprägte Toxizität der Substanz, die zu hämorrhagischer Zystitis, Blasenkrebs und Knochenmarksdepression führen kann. Für MMF gibt es aus anderen Untersuchungen an ILD-Patienten Hinweise, dass es auch bei RA-ILD Lungenfunktion und Beschwerden bessert.
DMARDs und Biologika sind aufgrund ihrer Lungentoxizität ein zweischneidiges Schwert. Zudem weiß man noch nicht, ob und wie diese Wirkstoffe eine RA-ILD beeinflussen. TNF-alpha-Blocker haben bekanntermaßen pro- und antifibrotische Wirkungen. In bisherigen Untersuchungen waren die Ergebnisse daher recht widersprüchlich. Ähnlich kontrovers sehen die Erfahrungen mit Rituximab aus, das prinzipiell durch seine B-Zell-Depletion durchaus bremsend auf eine RA-ILD wirken könnte.
Eine Option vor allem beim UIP-Muster bieten antifibrotische Medikamente. Bei anderen ILDs konnte Nintedanib Besserungen zeigen. Ob dies auch auf RA-ILD-Patienten zutrifft, steht nicht fest. Pirfenidon senkt die Spiegel von IL-6 und TNF-alpha und hatte in RA-ILD-Gewebeproben einen hemmenden Einfluss auf die Fibroblasten. Ein positiver Effekt, vor allem beim UIP-Muster, scheint deshalb den Autoren zufolge möglich.
Ultima Ratio bleibt die Lungentransplantation
Sind die Atemwege von einer RA beeinträchtigt, stehen andere Therapieoptionen an. Bronchiektasen werden behandelt wie „normale“ Bronchiektasen, also mit Bronchodilatatoren, Bronchialtoilette und Antibiotika. Die äußerst seltenen und mit schlechter Prognose behafteten Bronchiolitiden erfordern dagegen langwirkende Betamimetika und systemische Glukokortikoide. Zudem sollen einigen Kasuistiken zufolge Makrolide günstig wirken.
Neben den medikamentösen Behandlungsmöglichkeiten haben Rauchverzicht, pulmonale Rehabilitation, Sauerstoffgabe und die Behandlung eventueller Komorbiditäten, beispielsweise einer pulmonalen Hypertonie, entscheidende Bedeutung. Lässt sich die Erkrankung auf diese Weise nicht bremsen, kommt schlussendlich eine Lungentransplantation infrage.
Quelle: Kadura S, Raghu G. Eur Respir Rev 2021; 30: 210011; DOI: 10.1183/16000617.0011-2021
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).