Morbus Waldenström: Rutscht Ibrutinib in die zweite Reihe?
 Morbus Waldenström spricht auf den neuen BTK-Inhibitor an – Nebenwirkungen sinken.
© iStock/Dmitrii_Guzhanin
Morbus Waldenström spricht auf den neuen BTK-Inhibitor an – Nebenwirkungen sinken.
© iStock/Dmitrii_Guzhanin
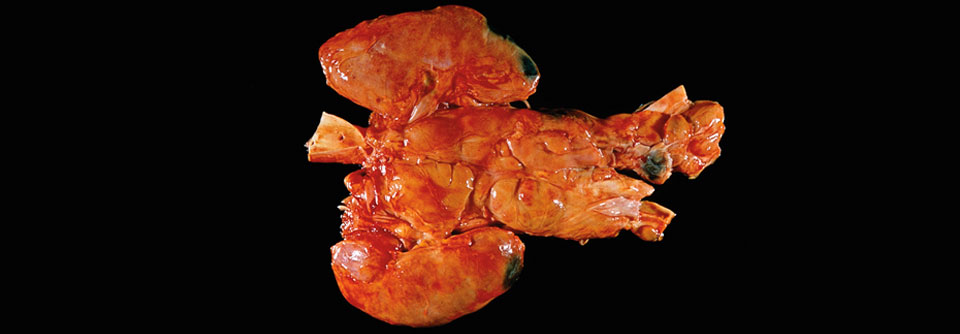
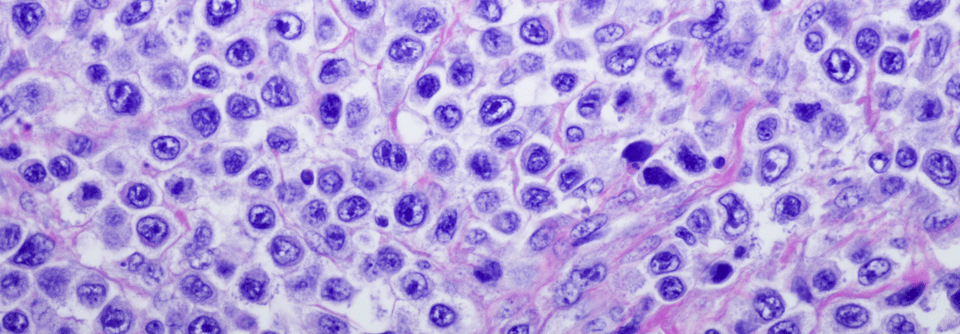
Der Morbus Waldenström ist ein seltenes indolentes Non-Hodgkin-Lymphom mit Knochenmarksinfiltration und monoklonaler Gammopathie im Serum. Die derzeit bedeutsamste genetische Alteration ist die L265P-Mutation im MYD88-Gen, das an der angeborenen und erworbenen Immunantwort beteiligt ist und im mutierten Zustand antiapoptotisch wirkt.
Zanubrutinib wirkt selektiver als Ibrutinib
Eine der wichtigsten therapeutischen Entwicklungen in den letzten Jahren war die Einführung des BTK-Inhibitors Ibrutinib. Der Zweitgenerations-BTK-Inhibitor Zanubrutinib ist selektiver und mindestens so wirksam wie Ibrutinib. Dieser wurde in den USA bereits zur Behandlung des rezidivierten oder refraktären…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.