Startschuss für neuen ALK-Inhibitor
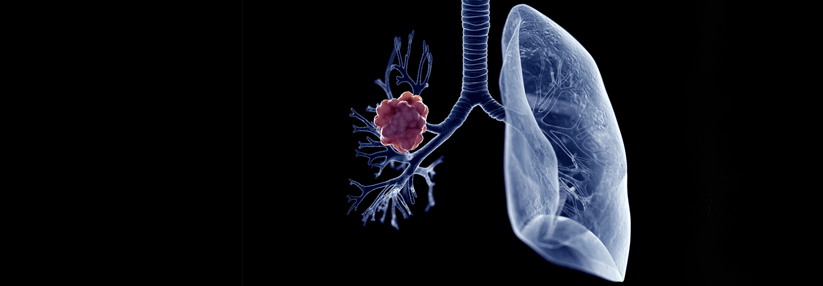
 4–5 % aller NSCLC weisen ein Rearrangement mit Beteiligung des ALK-Gens auf.
© Science Photo Library/Gschmeissner, Steve
4–5 % aller NSCLC weisen ein Rearrangement mit Beteiligung des ALK-Gens auf.
© Science Photo Library/Gschmeissner, Steve
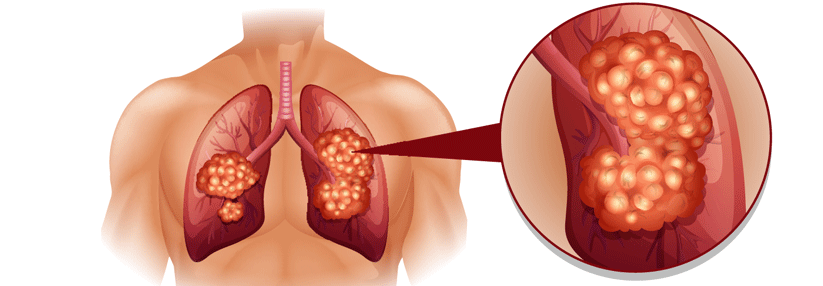
Seit vor zehn Jahren Crizotinib als erster ALK-Inhibitor zugelassen wurde, gehört die Testung auf Rearrangements des Gens zu den Standardprozeduren in der Diagnostik des NSCLC. Weil sich mit der Zeit eine Resistenz entwickelt und die Substanz eine beschränkte Liquorgängigkeit aufweist, wurde eine Reihe weiterer TKI entwickelt und zugelassen. Davon erwiesen sich einige – Alectinib, Brigatinib und Lorlatinib – gegenüber Crizotinib in der Erstlinientherapie als überlegen. Mit Ensartinib kommt nun der vierte Wettbewerber: Nach ersten positiven Daten aus Phase-1/2-Untersuchungen testeten Kollegen um Professor Dr. Leora Horn vom Vanderbilt-Ingram Cancer Center in Nashville den Wirkstoff in der Phase-3-Studie eXalt3. Eingeschlossen waren 290 Patienten mit ALK-positivem NSCLC, die zuvor keinen ALK-Inhibitor erhalten hatten.
Die Autoren randomisierten die aus 120 Zentren in 21 Ländern stammenden Teilnehmer zu entweder 225 mg Ensartinib einmal täglich oder zu 250 mg Crizotinib zweimal am Tag. Primärer Endpunkt war das durch ein unabhängiges und verblindetes Expertenkomitee festgestellte progressionsfreie Überleben (PFS).
Mehr als zwei Jahre progressionsfrei
In der Interimsanalyse der Intention-to-treat(ITT)-Population verdoppelte sich der PFS-Medianwert unter der Prüfsubstanz auf 25,8 Monate vs. 12,7 Monate in der Kontrolle (Hazard Ratio 0,51; p < 0,001). In einer modifizierten ITT-Population, für die der ALK-Fusionsstatus in einem zentralen Labor bestätigt wurde, fiel der Medianwert in der Crizotinib-Gruppe mit 12,7 Monaten identisch aus, während er im Interventionsarm noch nicht erreicht war (HR 0,45; p < 0,001). Hinsichtlich dem Gesamtüberleben, einer der sekundären Endpunkte, konnten die Autoren nach median zwei Jahren Nachbeobachtung noch keinen Unterschied feststellen.
Die intrakranielle Ansprechrate wurde ausweislich der Beurteilung durch ein verblindetes unabhängiges Gremium von 21,1 % unter Crizotinib auf 63,6 % unter Ensartinib verdreifacht, schreiben die Wissenschaftler. In der Patientengruppe, die zu Beginn keine Hirnmetastasen aufgewiesen hatte, war das mediane PFS noch nicht erreicht gegenüber 16,6 Monaten unter Crizotinib. Die Progressionsrate im Gehirn betrug nach zwölf Monaten im experimentellen Arm 4,2 % und in der Kontrolle 23,9 % (HR 0,32; p = 0,001).
Mit 7,7 % gegenüber 6,1 % litten nahezu gleich viele Teilnehmer unter der Prüfsubstanz vs. Kontrolle an schweren Nebenwirkungen. Auch Dosisreduktionen und Therapieabbrüche kamen mit 23,8 % gegenüber 19,9 % bzw. 9,1 % vs. 6,8 % in den beiden Gruppen ähnlich häufig vor.
Hautausschläge und erhöhte Leberenzyme
Unter Ensartinib traten vor allem Hautausschläge und Leberenzymerhöhungen auf, die aber meist niedriggradig ausfielen. Neue Sicherheitssignale gab es nicht. Mit diesen Ergebnissen dürfte der neue Tyrosinkinasehemmer – eine Zulassung vorausgesetzt – als neue Erstlinienoption für das ALK-positive NSCLC infrage kommen, schlussfolgern die Autoren.
Quelle: Horn L et al. JAMA Oncol 2021; 7: 1617-1625; DOI: 10.1001/jamaoncol.2021.3523
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).