Nebenwirkungen von Immuncheckpoint-Inhibitoren erstmals großflächig verglichen
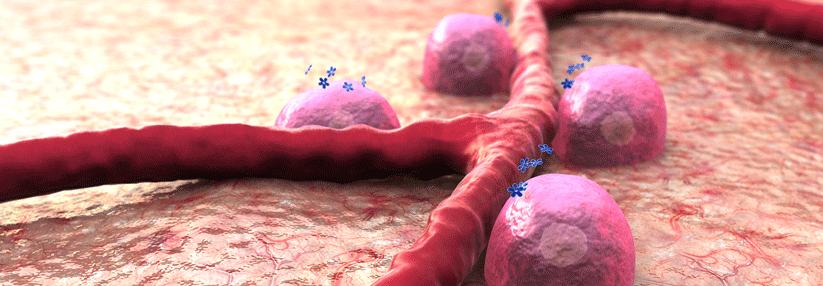
 Immuncheckpoint-Inhibitoren, die gegen PD1 (rot) oder PD-L1 (gelb) gerichtet sind, erfahren inzwischen eine verbreitete Anwendung.
© iStock/selvanegra
Immuncheckpoint-Inhibitoren, die gegen PD1 (rot) oder PD-L1 (gelb) gerichtet sind, erfahren inzwischen eine verbreitete Anwendung.
© iStock/selvanegra
Angesichts der mittlerweile weit verbreiteten Anwendung von PD1- und PD-L1-Inhibitoren wäre es von großer Bedeutung, ihr toxikologisches Profil und gegebenenfalls Unterschiede zwischen den einzelnen Substanzen genauer definieren zu können, schreiben die Wissenschaftler um Dr. Yucai Wang von der Mayo Clinic in Rochester. Auch wenn es bereits eine Vielzahl von klinischen Studien mit Immuncheckpoint-Inhibitoren gibt, müsse man zur Auswertung der Nebenwirkungsmuster für eine Metaanalyse besonders ausgefeilte statistische Methoden anwenden, um Verzerrungen der wahren Häufigkeiten von Toxizitäten zu vermeiden.
Die Studienautoren führten daher zunächst eine ausgedehnte Literaturrecherche durch, aus der sie alle klinischen Studien extrahierten, in denen PD(-L1)-Inhibitoren in Monotherapie eingesetzt und die behandlungsbedingten Nebenwirkungen tabellarisch wiedergegeben worden waren. Darüber hinaus wurden Tumortyp und Dosierungsschemata der Medikamente berücksichtigt. Unter Verwendung eines bayesianischen statistischen Modells wurde versucht, trotz fehlender Informationen in der einen oder anderen Studie ein repräsentatives Bild der Häufigkeit von Nebenwirkungen zu erhalten.
Der Wirkmechanismus
Zwei Drittel der Patienten mit Nebenwirkungen
Insgesamt konnten 125 klinische Studien mit über 20 000 Patienten identifiziert werden: In 106 dieser Studien mit insgesamt 18 610 Teilnehmern fanden sich Angaben zu mindestens einer Nebenwirkung beliebigen Schweregrads bei 66 % der Patienten. In insgesamt 110 Studien wurde bei 14 % der 18 715 Patienten wenigstens eine Nebenwirkung vom Grad 3 oder höher berichtet. Bezüglich der Toxizitäten aller Schweregrade überwogen- Fatigue (18,26 %),
- Pruritus (10,61 %) und
- Diarrhö (9,47 %).
- Fatigue (0,89 %),
- Anämie (0,78 %) sowie
- eine Erhöhung der Aspartat-Aminotransferase (0,75 %).
Ein Überblick
- Pembrolizumab
- Nivolumab
- Avelumab
- Atezolizumab
- Durvalumab
Unter PD1-Hemmern häufiger schwere Nebenwirkungen
PD1-Inhibitoren als Klasse wiederum waren mit einer deutlich höheren mittleren Inzidenz von höhergradigen unerwünschten Ereignissen assoziiert als PD-L1-Inhibitoren (OR 1,58; 95%-KI 1,00–2,54). Die Inzidenz der Nebenwirkungen war aber unabhängig von der Art des mit den Medikamenten behandelten Tumors.Beachten, dass kein Head-to-Head-Vergleich vorliegt!
Das Fazit der Autoren: Trotz weitgehend identischem Wirkmechanismus unterscheiden sich PD1- und PD-L1-Antikörper teilweise überraschend deutlich in der Häufigkeit, mit der sie Nebenwirkungen geringen und höheren Grades auslösen. Die umfangreiche Datensammlung, die in dieser Metaanalyse verarbeitet wurde, liefert Informationen, die für die Anwendung dieser Medikamente in der Praxis von Bedeutung sein könnte, so ihr Resümee. Allerdings sollte beachtet werden, dass es sich nicht um Head-to-Head-Vergleiche zwischen den verschiedenen Präparaten handelt.Quelle: Wang Y et al. JAMA Oncol 2019; doi: 10.1001/jamaoncol.2019.0393
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).