Neuer Standard in der CLL-Erstlinie bei älteren Patienten?
 Der Wirkmechanismus von Acalabrutinib ähnelt zwar dem von Ibrutinib, der Inhibitor bindet jedoch selektiver.
© molekuul.be – stock.adobe.com; iStock/PeopleImages
Der Wirkmechanismus von Acalabrutinib ähnelt zwar dem von Ibrutinib, der Inhibitor bindet jedoch selektiver.
© molekuul.be – stock.adobe.com; iStock/PeopleImages
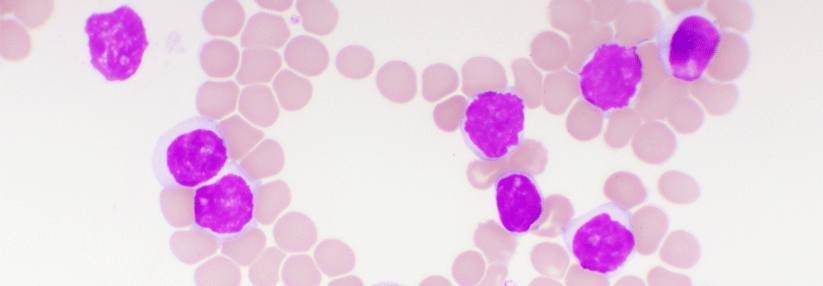
Die Bruton-Tyrosinkinase-Inhibitoren haben die Therapie der chronisch lymphatischen Leukämie (CLL) grundlegend verändert. Ein neuer Kandidat ist Acalabrutinib, der stärker selektiv wirkt als Ibrutinib. Deshalb wird der Inhibitor in der ELEVATE-TN-Studie bei älteren oder komorbiden Patienten mit CLL als Erstlinientherapie alleine und in Kombination mit Obinutuzumab geprüft. Nun liegen Interimsergebnisse vor, von denen Dr. Jeff P. Sharman, Willamette Valley Cancer Institute, Eugene, berichtete.
Studiendesign
- Acalabrutinib (100 mg oral 2x/d; n = 79),
- Acalabrutinib + Obinutuzumab (1000 mg an Tag 1, 2, 8 und 15 in Zyklus 1 und danach jeweils an Tag 1 für fünf 28-tägige Zyklen; n = 179) oder
- Obinutuzumab + Chlorambucil (oral 0,5 mg/kg an Tag 1 und 15 für sechs 28-tägige Zyklen; n = 177).
Fast jeder Patient unter Kombination in Remission
Auch das Ansprechen fiel in den Acalabrutinib-Armen signifikant besser aus als unter der Kontrolle. Die Gesamtansprechrate (ORR) lag im alten Standard bei 78,5 %, unter Acalabrutinib bei 85,5 % (p = 0,0763 vs. Obinutuzumab/Chlorambucil) und unter Acalabrutinib/Obinutuzumab bei 93,9 % (p < 0,0001 vs. Obinutuzumab/Chlorambucil). Obwohl Patienten bei Progress vom Standard zu Acalabrutinib wechseln konnten, zeichnet sich bereits eine geringere Sterblichkeit unter Monotherapie ab, erläuterte Dr. Sharman. Aktuell fallen die Ereignisraten aber noch zu gering aus, um einen signifikanten Überlebensvorteil zu belegen.Nebenwirkungen traten häufig auf
* progressionsfreies Überleben
Quellen:
1. Sharman JP et al. ASH Annual Meeting 2019; Abstract #31
2. Ghia P et al. 24. EHA-Kongress 2019; Abstract LB2606
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).