AML: IDH1-Inhibitor führt in Phase-I-Studie zu Komplettremissionen
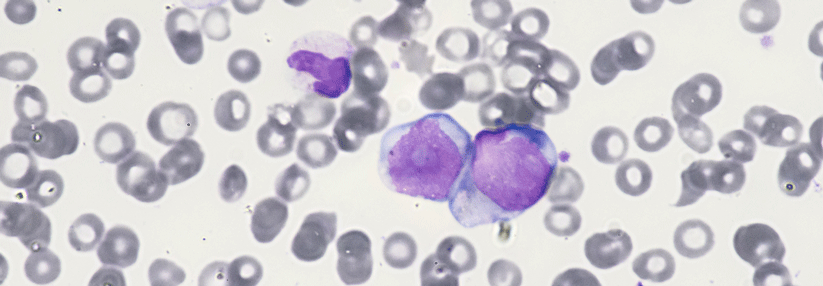
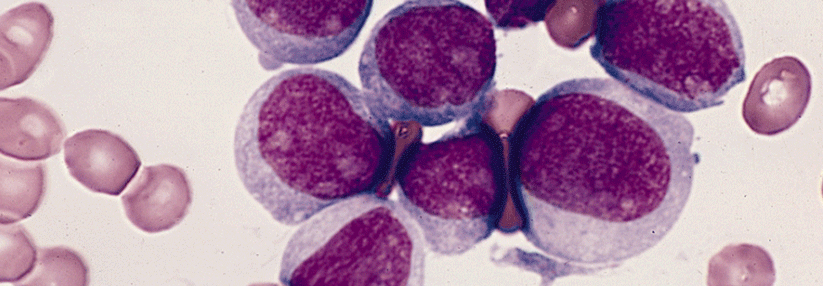 Der Inhibitor erweist sich bei Patienten mit rezidivierter oder refraktärer, IDH1-mutierter AML als gut verträglich.
© Wikimedia/AFIP
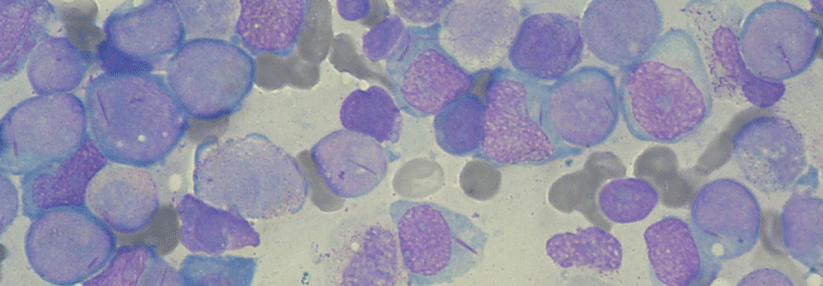
Der Inhibitor erweist sich bei Patienten mit rezidivierter oder refraktärer, IDH1-mutierter AML als gut verträglich.
© Wikimedia/AFIP
IDH1-Mutationen finden sich in 6–10 % aller AML-Fälle, IDH2 ist sogar bei 9–13 % der Patienten mutiert. Die mutierten Enzyme reduzieren a-Ketoglutarat zu dem Onkometaboliten 2-Hydroxyglutarat, was zu epigenetischen Veränderungen in den Zellen und zur Störung der hämatopoetischen Differenzierung führt.
Der IDH2-Inhibitor Enasidenib ist in den USA bereits zugelassen, während es zum IDH1-Inhibitor Ivosidenib bislang nur präklinische Daten gab. Erstmals wurde Ivosidenib nun in den USA und Frankreich in einer Phase-I-Studie bei insgesamt 258 Patienten mit IDH1-mutierter AML klinisch getestet. Die Nachbeobachtungszeit betrug mindestens sechs Monate.
Primäres Ziel einer Phase-I-Studie ist immer die Sicherheit. Folgende Nebenwirkungen vom Grad 3 oder höher traten bei jeweils mind. drei Patienten mit rezidivierter/refraktärer Erkrankung auf, die eine Dosierung von 500 mg/d erhielten:
- Verlängerung des QT-Intervalls (7,8 %)
- IDH-Differenzierungs-Syndrom (3,9 %)
- Anämie (2,2 %)
- Thrombozytopenie (3,4 %)
- Leukozytose (1,7 %)
In der primären Wirksamkeits-Population von 125 Patienten wurden 41,6 % Remissionen registriert, darunter 21,6 % komplette Remissionen und 8,8 % Komplettremissionen mit nur partieller hämatologischer Erholung. Im Median hatten sie eine Dauer von 6,5 Monaten, 9,3 Monaten und 8,2 Monaten.
Gut ein Drittel kann auf Blutkonserven verzichten
Von 84 ursprünglich transfusionspflichtigen Patienten wurden 29 (35 %) unabhängig von Blutkonserven, und die Patienten, die auf die Behandlung ansprachen, erlitten seltener Infektionen und febrile Neutropenien als die Non-Responder. Bei etwa jedem fünften der Patienten mit kompletter Remission (mit oder ohne vollständige hämatologische Erholung) war mittels hochsensitiver Polymerasekettenreaktion keine minimale Resterkrankung, d.h. keine IDH1-Mutation, mehr nachweisbar. Es konnten keine weiteren, gleichzeitig auftretenden Mutationen identifiziert werden, die ein klinisches Ansprechen oder eine Resistenz gegenüber der Therapie hätten anzeigen können.
Inhibitor scheint anderenTherapien überlegen
Ivosidenib erweist sich also bei Patienten mit rezidivierter oder refraktärer, IDH1-mutierter AML als gut verträglich. Da es bei einem Teil der Patienten zur Transfusionsunabhängigkeit sowie zu andauernden und gelegentlich sogar molekularen Komplettremissionen führt, scheint es anderen Therapien überlegen, lautet das Urteil der Wissenschaftler.
Quelle: DiNardo CD et al. N Engl J Med 2018; 378: 2386-2398
Ivosidenib in weiteren Studien
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).