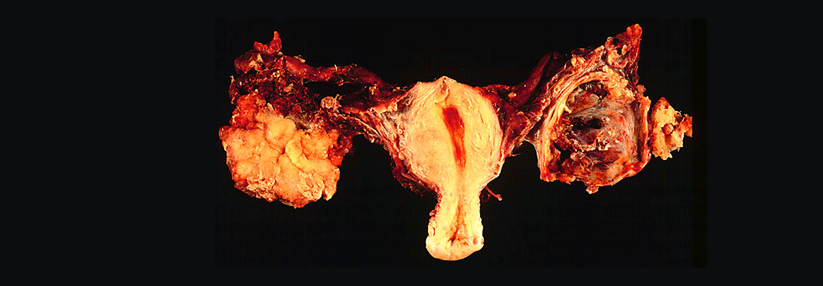
Ovarialkarzinom: PARP-Inhibitor auch bei Heterozygotie-Verlust effektiv
 Der PARP-Inhibitor könnte bei rezidiviertem Ovarialkarzinom breiter eingesetzt werden.
© iStock/magicmine
Der PARP-Inhibitor könnte bei rezidiviertem Ovarialkarzinom breiter eingesetzt werden.
© iStock/magicmine
Die meisten Patientinnen mit Ovarialkarzinom im fortgeschrittenen Stadium zeigen auf eine initiale platinbasierte Chemotherapie ein Ansprechen, auf das aber in der Regel nach einiger Zeit ein Rezidiv folgt. Wenn dieses Rezidiv wieder auf eine Platintherapie anspricht, erhalten die Patientinnen heute regelmäßig als Erhaltungstherapie einen Inhibitor der Poly(ADP-Ribose-)Polymerase (PARP), mit dem das progressionsfreie Überleben (PFS) signifikant verlängert werden kann.
Der PARP-Inhibitor Rucaparib ist in den USA bereits für die Erhaltungstherapie bei Vorliegen einer BRCA-Mutation zugelassen. In einer der relevanten Studien hatte Rucaparib aber nicht nur bei Vorliegen dieser Mutationen ein Ansprechen erbracht, sondern auch bei Tumoren mit BRCA-Wildtyp, die einen Verlust an Heterozygotie aufweisen. Das ist wiederum ein Marker für einen Defekt in der homologen Rekombination, bei dem PARP-Hemmer ebenfalls wirksam sind.
Heterozygotie-Verlust unter die Lupe genommen
In der Phase-III-Studie ARIEL3 sollte deshalb noch einmal getestet werden, wie wirksam und sicher Rucaparib als Erhaltungstherapie nach einem Ansprechen auf eine platinbasierte Therapie in der Zweit- oder einer höheren Therapielinie ist. Ein besonderes Augenmerk wurde darauf gelegt, wie sich der Grad eines Heterozygotie-Verlusts (LOH) auf die Sensitivität gegenüber dem PARP-Inhibitor auswirkt.
In die Studie wurden 564 Patientinnen mit Ovarial-, primär peritonealem oder Tubenkarzinom eingeschlossen, die auf eine platinbasierte Chemotherapie mit mindestens einer partiellen Remission angesprochen hatten. Sie wurden im Verhältnis 2:1 randomisiert, in doppelblinder Manier zweimal täglich 600 mg Rucaparib oral oder Placebo zu erhalten.
Primärer Endpunkt war das von den Prüfärzten attestierte PFS. Dieses wurde zunächst nur für die Patientinnen mit BRCA-Mutationen, dann für die mit defekter homologer Rekombination (BRCA-Mutationen oder BRCA-Wildtyp bei gleichzeitigem hohem Heterozygotie-Verlust) und schließlich für die gesamte Intention-to-treat-Population bestimmt.
Bei den Patientinnen mit mutierten BRCA-Genen konnte Rucaparib – wie auch von anderen PARP-Inhibitoren bekannt – das PFS von median 5,4 auf 16,6 Monate verdreifachen (HR 0,23; p < 0,0001). Bei den Patientinnen mit Defekten der homologen Rekombination (BRCA-Mutation oder starker LOH) war der Effekt etwas geringer, aber mit 13,6 vs. 5,4 Monaten immer noch sehr ausgeprägt (HR 0,32; p < 0,0001). In der Gesamtpopulation gab es eine Verdoppelung des medianen PFS von 5,4 auf 10,8 Monate (HR 0,36; p < 0,0001). Auch die Patientinnen mit BRCA-Wildtyp und niedriger LOH hatten einen gewissen Nutzen von Rucaparib: Mehr als 30 % von ihnen blieben mehr als ein Jahr progressionsfrei, während es im Placeboarm nur 5 % waren.
Nebenwirkungen steigen an
Quelle: Coleman RL et al. Lancet 2019; 390: 1949-61
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).