Duale CAR-T-Zellen plus Checkpoint-Inhibitor gegen das rezidivierte DLBCL
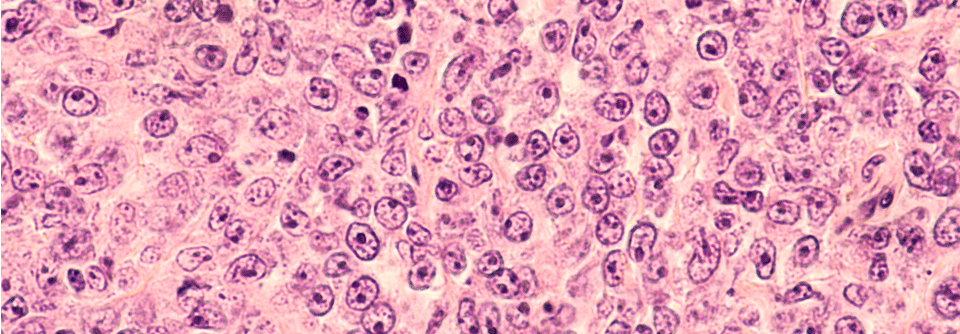
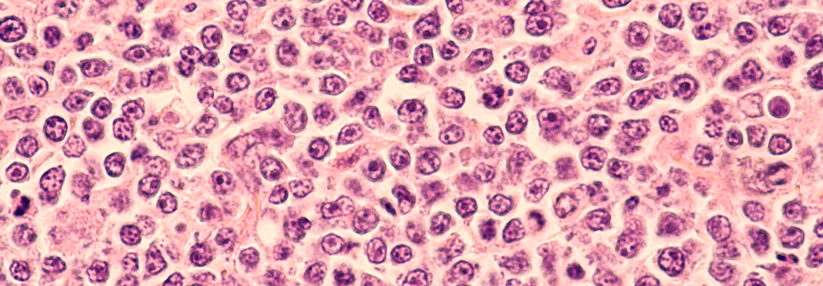
 Das DLBCL hat eine jährliche Inzidenz von ca. 7 Fällen pro 100 000 Einwohner. Männer sind häufiger betroffen als Frauen.
© wikimedia/Nephron (CC BY-SA 3.0)
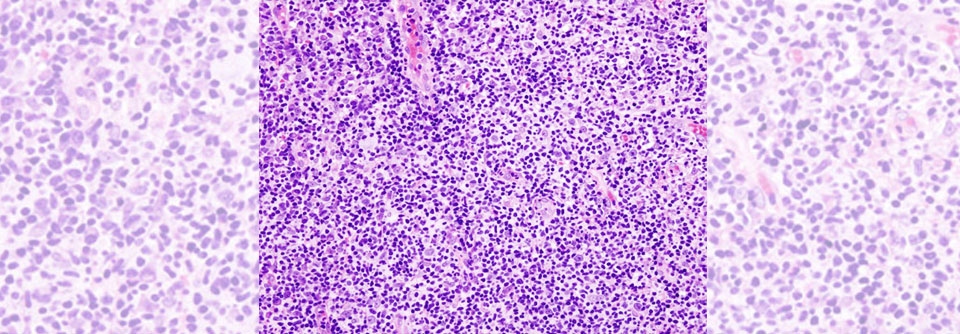
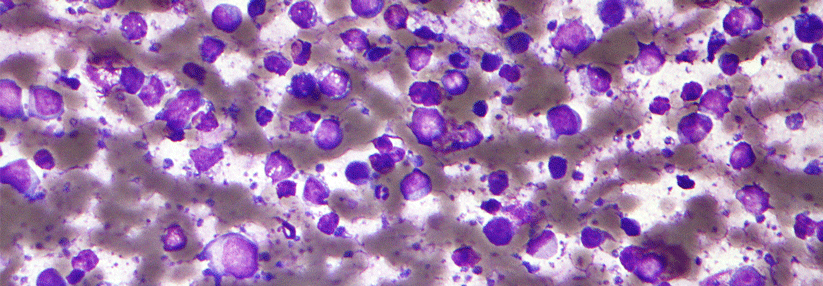
Das DLBCL hat eine jährliche Inzidenz von ca. 7 Fällen pro 100 000 Einwohner. Männer sind häufiger betroffen als Frauen.
© wikimedia/Nephron (CC BY-SA 3.0)
Die bisher in der Behandlung des rezidivierten oder refraktären diffus-großzelligen B-Zell-Lymphoms (DLBCL) verwendeten Anti-CD19-CAR-T-Zellen zeigen zunächst hohe Raten an Remissionen. Sie sind jedoch teilweise nicht von Dauer, denn langfristig bleibt nur etwa ein Drittel der Patienten in einer kompletten Remission. Zu den wichtigsten Resistenzmechanismen gehören der Verlust des CD19-Antigens auf den Lymphomzellen („antigen escape“) und ihre Expression des Checkpoint-Liganden PD-L1, der die Aktivität der T-Zellen unterdrückt.
In ALEXANDER, einer britisch-US-amerikanischen Phase-1/2-Studie, versucht man beide Probleme zu umgehen: Die verwendeten CAR-T-Zellen tragen chimäre Antigenrezeptoren nicht nur gegen CD19, sondern auch gegen das ebenfalls auf B-Zellen exprimierte CD22-Antigen. Zusätzlich nutzt man den PD1-Antikörper Pembrolizumab. Das als AUTO3 bezeichnete CAR-T-Zell-Präparat wurde in steigenden Dosierungen von 50, 150 und 450 x 106 Zellen gegeben, Pembrolizumab in einer Dosis von 200 mg entweder einmal am Tag der Zelltherapie oder ab zwei Wochen danach mit drei Dosen im Abstand von drei Wochen.
Dosislimitierende Toxizitäten traten nicht auf
Wie Dr. Eleni Tholouli von der Manchester University berichtete, haben bisher 35 Patienten teilgenommen. Primärer Endpunkt umfasste, wie in einer Phase 1 üblich, die Häufigkeit von dosislimitierenden Toxizitäten und Nebenwirkungen vom Grad 3–5. Sekundäre Endpunkte waren die Rate von Gesamtansprechen und Komplettremissionen sowie Biomarkermessungen.
Unter keiner Dosierung der CAR-T-Zellen registrierten die Wissenschaftler dosislimitierende Toxizitäten. Die Mehrzahl der schweren Nebenwirkungen von mindestens Grad 3 war hämatologischer Natur (Neutropenien 87 %, Thrombozytopenien 57 %, Anämien 48 %) und reversibel.
Ein Zytokin-Release-Syndrome von mindestens Grad 3 trat auch in höheren Dosierungen nicht auf. Jedoch bekamen fünf Patienten mit einem niedriggradierem Syndrom Tocilizumab. Neurotoxizitäten entwickelten drei Teilnehmer, davon zwei mindestens Grad 3.Alle drei Fälle waren atypisch und traten unter einer Krankheitsprogression und ohne Expansion der CAR-T-Zellen sowie unter Umständen wie Sepsis oder metabolischer Azidose auf. Patienten in Remission, die eine robuste CAR-T-Zell-Präsenz aufwiesen, entwickelten keinerlei Neurotoxizitäten.
Von den 28 bisher auswertbaren Patienten hatten 19 (68 %) angesprochen, 15 davon (54 %) mit einer Komplettremission. Eine Subgruppe von 14 Erkrankten hatte mit mindestens 150 x 106 Zellen die empfohlene Dosis für die Phase 2 und Pembrolizumab als Einzeldosis erhalten. Sie schnitten der Referentin zufolge zumindest nicht schlechter ab mit insgesamt 71 % Remissionen und 64 % Komplettremissionen. Von den 15 Komplettremissionen, so Dr. Tholouli, dauern 14 noch an, im Median seit sechs Monaten; der längste Verlauf beträgt zwei Jahre. AUTO3 scheint der Kollegin zufolge besser verträglich zu sein als die bislang verfügbaren autologen CAR-T-Zell-Produkte, und das bei „ausgezeichneter Wirksamkeit“.
Quelle: Tholouli E et al. ESMO Virtual Congress 2020; Abstract 890MO
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).